Tartalom
Az endocitózis fogalma a külvilág felől a sejt belsejébe vezető, membránbefűződéssel és –leválással járó, vezikulák által közvetített anyagfelvételi utak összességét jelöli. A lipid kettősrétegen keresztül, transzmembrán transzporttal a sejt számára szükséges anyagok csak igen kis hányada képes átjutni. Valamennyi egyéb tápanyag vezikuláris transzporttal jut el a lizoszómáig, ahol lebontásra kerül, és komponensei a citoszolba jutnak hasznosítás céljából.
Az endocitózis során azonban korántsem jut valamennyi felvett anyag a lizoszómába, funkciója egyáltalán nem korlátozódik a tápanyagfelvételre. A sejt életének más területein is fontos szerepet játszik: részt vesz a védekezésben, a jelátviteli folyamatok szabályozásában. A szekréció utolsó lépésekor, az exocitózis során jelentős membrántöbblet keletkezhet a sejt felszínén, amelyet vissza kell juttatni a donor sejtszervecskéhez – ezt szintén endocitózis biztosítja. A vírusok és sejtes patogének többsége is az endocitózis folyamatában szerepet játszó apparátust használja ki a fertőzés során.
A sejt belsejébe irányuló transzport által szállított molekulák az endocitotikus kompartmentekbe kerülnek. Első lépésben valamennyi lefűződő vezikula egy korai endoszómával fuzionál, amely a TGN-hez hasonlóan (lásd 9. fejezet) elosztóállomásként működő, rendkívül dinamikus, folyamatosan változó organellum. Nemcsak az extracelluláris térből fogad anyagokat, hanem a TGN felől is érkeznek lizoszomális enzimeket és membránfehérjéket szállító vezikulák – emellett visszafelé irányuló retrográd transzport biztosítja a receptorok és más membrán komponensek visszaszállítását a TGN-be. A korai endoszóma komponenseinek egy része vezikuláris transzporttal - közvetlenül vagy reciklizáló endoszómák közbeiktatásával – exocitózis révén visszakerül a plazmamembránba vagy az extracelluláris térbe, más részük pedig késői endoszómába jut, amely a lizoszómába vezető út közbülső állomása. A korai endoszómára is, de főleg a késői endoszómára jellemző a lumenben lokalizálódó belső (intraluminális) vezikulák jelenléte, ami miatt multivezikuláris testeknek (multivesicular body, MVB) is nevezik ezeket a képleteket (1. ábra).
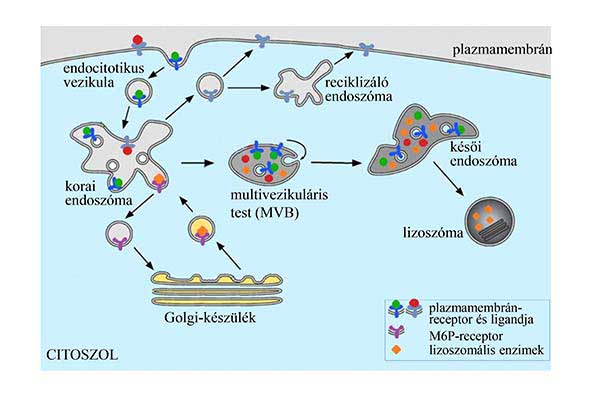
1. ábra A sejt endocitózisban részt vevő belső terei és az endocitózis folyamata kétféle plazmamembrán-receptor sorsának példáján. Az ábrán egy szekrécióhoz tartozó lépés, a mannóz-6-foszfát receptor (M6P) által a lizoszómába szállított enzimek útja is fel van tüntetve. MVB: multivezikuláris test (multivesicular body).
Az endocitózis tanulmányozását segíti, hogy a transzport kiinduló állomása a kísérletesen könnyedén manipulálható extracelluláris tér. Fluoreszcensen vagy egyéb módon jelölt oldott molekulák, különböző méretű részecskék, receptorok, ligandok, membránalkotók alkalmazásával követhető a sejtbe jutott anyag további sorsa. A folyamat élesztősejtekben az állati sejtekhez nagyon hasonlóan játszódik le, központi vakólumuk megfeleltethető a lizoszómának. Hosszú ideig az emlős szövettenyészeteken kívül ebben a modellrendszerben végezték a legtöbb kísérletet (számos, az endocitózisban és egyéb, a lizoszómális transzportban szerepet játszó géntermék neve is innen származik: Vps – vacuolar protein sorting). Újabban más, erős genetikai háttérrel rendelkező modellszervezetben – Caenorhabditis elegans, Drosophila melanogaster – is intenzíven kutatják.
Az endocitózis tehát valamennyi sejt életében esszenciális, az exocitózissal szorosan kapcsolt folyamat. A vezikulák képződésének, sejten belüli mozgásának, fúziójának általános molekuláris mechanizmusával, az abban résztvevő fehérjékkel kapcsolatos mai ismereteinket az 8. fejezet mutatja be. Az endocitózis bizonyos szakaszainak megértéséhez pedig hasznos, ha az olvasó a szekréciót tárgyaló 9. fejezetet is áttanulmányozza. Mindkét anyagrészre többször utalunk majd.
Valamennyi sejt folyamatosan vesz fel a környezetéből vezikulákba zárva folyadékot és benne többek között oldott tápanyagokat, az extracelluláris mátrix komponenseit; valamint membránösszetevőket: lipideket és membránfehérjéket. Ezt a jelenséget pinocitózisnak, „folyadékivásnak” nevezik (2. ábra).
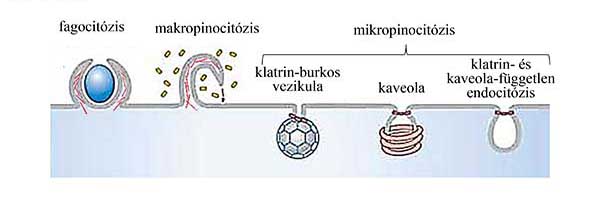
2. ábra Az endocitózis típusai. Az ábrán nem méretarányosan vannak feltüntetve a különböző mecahnizmusokkal kialakuló képletek: a fagocitózis és a makropinocitózis során lefűződő vezikulák mérete sokszorosan meghaladhatja a mikropinocitózissal keletkezőkét.
Mikropinocitózis során kis, nagyjából egyforma méretű (~100nm-es) vezikulák fűződnek le, elsősorban klatrin-burok kialakulásával (lásd 8. fejezet 6. ábra), de más, klatrin-független folyamatok is szerepet játszhatnak benne. A makropinocitózis jóval nagyobb, akár 0,5-5μm átmérőjű vezikulák keletkezésével jár, amelyekben a folyadék aránya sokkal nagyobb a pinocitózishoz képest.
A fagocitózis során nagyobb szilárd szemcsék, sejttörmelék, mikroorganizmusok bekebelezése történik, a keletkező fagoszómák mérete jóval nagyobb és változó, a felvett részecske mérete határozza meg. Egysejtűekben ez a táplálékszerzés egyik módja, soksejtűekben célja elsősorban a környezetben elpusztult sejtek „eltakarítása” és a védekezés. A hatékonyság érdekében ezt a feladatot az immunrendszer erre szakosodott sejtjei végzik. A fagocitózis a fentiek következtében nem is állandóan zajlik: speciális sejtfelszíni receptorok ismerik fel a bekebelezendő anyagot, és indukálják a folyamatot. Kezdetben állábszerű nyúlványokkal veszi körbe a fagocitáló sejt a részecskét, amely végül körbezárul, és a fagoszóma lefűződik - mindez ebben az esetben is az aktinváz intenzív átrendeződésével jár együtt (2. ábra).
A pinocitózis kategorizálható aszerint is, hogy milyen típusú burok játszik közre a vezikula képződésében. Ez a megkülönböztetés nemcsak morfológiai jelentőségű, hiszen, amint a vezikuláris transzport mechanizmusáról szóló 8. és a szekréciót bemutató 9. fejezetből is megtudható, a burkot létrehozó fehérjék szelektív kötődésekkel maguk is alakítják a vezikula tartalmának összetételét. A legrégebben és legintenzívebben kutatott terület a klatrin-burkos vezikulák lefűződésével járó endocitózis, a következőkben elsősorban az innen származó ismereteket mutatjuk be. Ugyanakkor egyre több eredmény születik az úgynevezett kaveolákkal, illetve más, klatrin-független endocitózissal kapcsolatban is, amellyel egy külön alfejezet foglalkozik.
Egyes tankönyvekben a fago- és pinocitózis mellett harmadik típusként szokták a receptor-mediált endocitózist emlegetni. Valójában ez egy független kategória, bár kétségtelen, hogy leginkább a mikropinocitózissal kapcsolatban tudunk a legtöbbet róla. Általában ugyanis kisméretű vezikulák lefűződésével jár, amelyet legtöbbször klatrin burkol; de célja nem aspecifikus folyadék- és membránfelvétel, hanem bizonyos plazmamembrán-receptorok és/vagy ligandjaik kiválogatása (3. ábra).
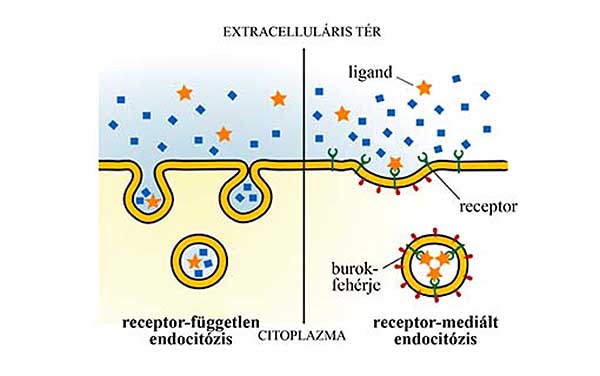
3. ábra A receptorok által közvetített endocitózis során specifikusan, nagy hatékonysággal tud a sejt anyagokat felvenni az extracelluláris térből.
A receptor-mediált endocitózissal tehát kis térfogatban, de nagy hatékonysággal lehet az extracelluláris térben vagy a membránban akár igen alacsony koncentrációban jelen lévő makromolekulákat a sejtbe juttatni - például a membránalkotó koleszterin felvétele is így zajlik.
A receptor endocitózisa lehet konstitutív, mint egyes alapanyagok szállításáért felelős receptorok esetében (LDL-, transzferrin-receptor – lásd később); ekkor a receptor ligand nélkül is internalizálódhat. Legtöbbször azonban a receptor-ligand kölcsönhatás létrejötte indukálja a vezikulába jutást, és célja sok esetben éppen az, hogy a receptort rövidebb-hosszabb időre „kivonja a forgalomból”. Az életműködéshez szükséges, kis koncentrációjú molekulák bejuttatásán kívül tehát a receptor-mediált endocitózisnak óriási szerepe van a transzmembrán receptorokon keresztül történő jelátvitel szabályozásában is. A fejezetben bemutatott, endocitózissal kapcsolatos ismeretek többsége is a receptor-mediált endocitózis vizsgálatából ered.