Több laboratóriumban nagy mutánsgyűjteményeket hoztak létre élesztőben. A mutáns törzsek közül azokat keresték, amelyek az éheztetés hatására elpusztultak. Az élesztő éheztetésre autofágiával válaszol, hogy ilyen módon jusson tápanyagokhoz. Ha a mutáció következtében az autofágia gátolt, akkor elpusztul. Az ilyen törzsekben azonosították a mutáció által érintett gént és meghatározták, hogy mi a szerepük az autofágia során. E géneket „autophagy related” („Atg”) géneknek nevezték el. Ma 34 Atg gént ismerünk. Ezek a funkciójuk alapján több csoportba sorolhatók. Részletes ismertetésüktől itt eltekintünk, de a 3. ábrán bemutatjuk, hogy az egyes géncsoportok az autofágia mely lépéseit szabályozzák. Vannak közöttük olyanok, amelyek a preautophagosomalis komplex létrejöttéhez (nucleatio), vagy az izoláló membrán megnyúlásához (elongatio), vagy az izoláló membrán bezáródásához (completition), vagy az autofagoszóma-lizoszóma fúzióhoz (fusion) és olyanok, amelyek a degradációhoz szükségesek.
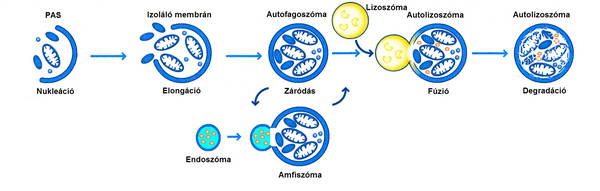
10. ábra. Az autoliszoszóma kialakulásához vezető lépések
Ugyancsak ezek a genetikai vizsgálatok mutattak rá arra, hogy az autofágia beindulása (elsősorban a nucleatio lépése) döntően a TORC1 (target of rapamycin kinase complex 1) szabályozása alatt áll. A TORC1 alaphelyzetben gátolja a preautophagosomalis struktúra kialakításában részt vevő géntermékeket, azok foszforilált állapotban tartásával. Ha a TORC1 inaktiválódik a sejtben (pl. éheztetés hatására, vagy növekedési faktorok hiányában), az Atg fehérjék defoszforilálódnak és beindítják az autofágiát (egyidejűleg gátolják, vagy lassítják az anabolikus folyamatokat).
A TORC1 felé vezető legfontosabb szignalizációs út az inzulin/inzulin-szerű növekedési faktor jelátviteli útvonal. A növekedési faktor hiányára, vagy megvonására a sejtek autofágiával válaszolnak. Az inzulin-szerű növekedési faktor jelátviteli útban normális körülmények között az inzulin-szerű növekedési faktor kapcsolódik a sejtmembránban lévő receptorához. Ennek következtében foszforilálódik az inzulin receptor szubsztrát 1 és 2 (IRS1 és IRS2). Az IRS-ek aktiválják a foszfoinozitid 3-kinázt (class I PI3K), ami a sejtmembránban lévő foszfatidil-inozitol 4,5 difoszfátot foszforilálja. A PKB/Akt odakötődik a foszfatidil-inozitol 3,4,5 trifoszfáthoz és ennek hatására aktiválódik. A PKB/Akt a TSC2-t inaktiválja, hatására a TSC2 már nem képes komplexet képezni a TSC1-gyel. Ezért a TSC2 nem képes GDP-t kötő formában tartani a Rheb fehérjét, amely az mTORC1 egyik legfontosabb aktivátora. Az aktív Rheb megköti azt az FKBP38 fehérjét, ami a TORC1 inhibítora. Tehát amíg a növekedési faktor hat a sejtre, addig a TORC1 aktív állapotban van és gátolja az autofágiát, valamint fenntartja a sejt szintetikus folyamatainak működését (és a proliferációját is).
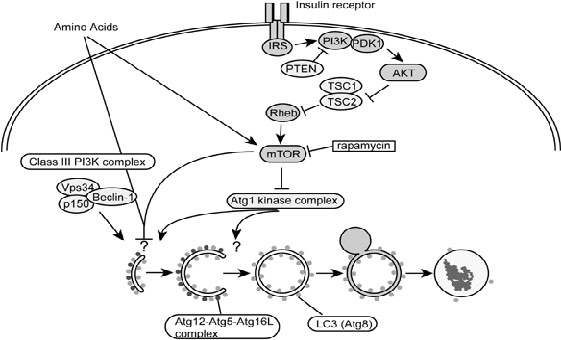
11. ábra. Az inzulin/inzulinszerű növekedési faktor jelátviteli útvonal
A TORC1 (mTOR), ahogy korábban is láttuk, elsősorban az Atg gének fehérjetermékeinek működését szabályozza, amelyek fontos szerepet játszanak az autofagoszóma kialakításában, növekedésében, továbbá elősegítik lizoszómákkal való fúziót is.